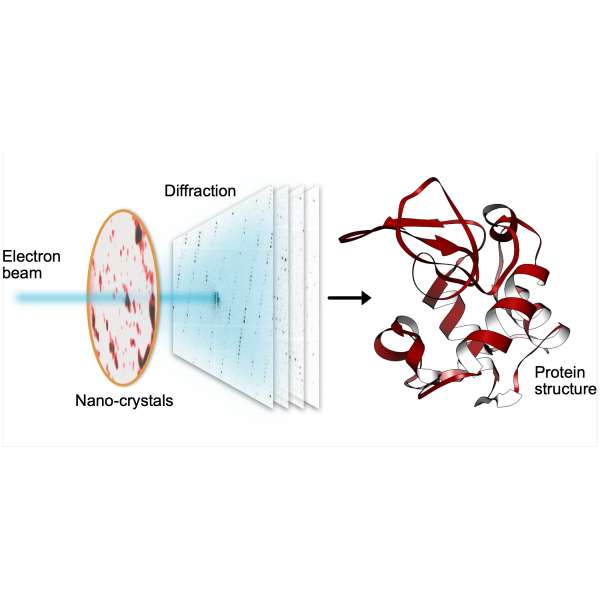
Elektronenbeugung zeigt winzige Kristalle in neuem Licht
Physik-News vom 24.02.2020
Um die biologischen Funktionen von Proteinen, den Bausteinen des Lebens, zu verstehen, ist es unerlässlich, ihre Struktur zu erforschen. Dank ihrer winzigen Dimensionen und Zerbrechlichkeit, sind diese Strukturen jedoch schwer zu bestimmen. Die immense Dosis an hochenergetischer Röntgenstrahlung, die Daten in ausreichender Auflösung erzeugt, richtet in den zu untersuchenden Proteinen jedoch große Schäden an, die oft genau diese Strukturauflösung verhindert.
Nun haben Forscher am Max-Planck-Institut für Struktur und Dynamik der Materie und dem Deutschen Elektronensychrotron (DESY) in Hamburg eine innovative neue Methode entwickelt, die diese Probleme umgeht und weit verbreitete, kosteneffektive Technologien nutzt. Ihre Beschreibung dieser Methode wurde in Nature Communications veröffentlicht.
Publikation:
Robert Bücker, Pascal Hogan-Lamarre, Pedram Mehrabi, Eike C. Schulz, Lindsey A. Bultema, Yaroslav Gevorkov, Wolfgang Brehm, Oleksandr Yefanov, Dominik Oberthür, Günther H. Kassier & R. J. Dwayne Miller
Serial protein crystallography in an electron microscope
Nature Communications volume 11, Article number: 996 (2020)
DOI: 10.1038/s41467-020-14793-0
Seit Jahrzehnten suchen Forscher aus diversen Feldern, von der Physik bis zur Biologie und Biochemie, nach kreativen Lösungen für das Strahlungsschäden-Problem. Ein neuer Ansatz ist die Nutzung von ultrakurzen und intensiven Röntgenblitzen an Großinstrumenten wie dem neuen European X-ray Free Electron Laser (EuXFEL) in Hamburg, welcher hochaufgelöste Abbildungen produziert, bevor die Proteine wortwörtlich explodieren.
Obwohl diese Methode durch spektakuläre Ergebnisse besticht, benötigt man große und teure Teilchenbeschleuniger, um Röntgenstrahlen der nötigen Brillianz zu erzeugen. Eine andere Methode setzt stattdessen Elektronenstrahlen ein, die sanfter mit den zarten Biomolekülen umgehen und einfacher zu erzeugen sind. Diese kommt zum Beispiel am Center for Structural Systems Biology (CSSB) in Hamburg zum Einsatz.
Die Forscher vom MPSD - am Center for Free-Electron Laser Science (CFEL) - und DESY haben nun auf raffinierte Weise diese Ansätze mit Big Data-Analysen und den neuesten Kameratechnologien kombiniert und dadurch hochaufgelöste Proteinstrukturen aus relativ leicht erhältlichen Nanokristallen gewonnen. Hierzu entwickelten die Wissenschaftlerinnen und Wissenschaftler die serielle Elektronenbeugung (Serial Electron Diffraction), die experimentelle Methoden aus der Röntgenkristallographie adaptiert, um Beugungsmuster aus tausenden Kristallen zu gewinnen und diese zu verarbeiten.
Statt ein Milliarden-Euro-Großforschungsinstrument wie den EuXFEL einzusetzen, verteilten sie diese Kristalle einfach auf einem dünnen Kohlefilm und legten sie in ein Elektronenmikroskop, wie es in vielen Laboren vorhanden ist. Der Elektronenstrahl wird dazu gebracht, von einem Nanokristall zum nächsten zu hüpfen, um Beugungsdaten zu sammeln. Die Nutzung von Nanokristallen reduziert nicht nur die benötigte Menge der oft seltenen und teuren Proben, sondern erspart den Forschern zudem das Züchten großer Proteinkristalle, wie bei konventionellen Röntgenmethoden – oftmals eine extrem schwierige Aufgabe.
Um die vom Elektronenstrahl verursachten Schäden zu umgehen, wird statt eines Einzelbildes ein kurzer Film mit einer Hochgeschwindigkeitskamera gedreht, während der Elektronenstrahl auf einem Kristall ruht. Der Film zeigt, wie der Kristall buchstäblich „dahinschmilzt“ und dennoch bleiben ausreichende Informationen im Diffraction during Destruction-Movie, um die Daten so zu rekonstruieren, als hätte es beinahe keinen Schaden gegeben. Dieser Prozess wird innerhalb weniger Stunden bei tausenden von Nanokristallen wiederholt, die enormen Datenmengen werden dann mithilfe am DESY entwickelter, spezieller Software in eine hochaufgelöste Proteinstruktur umgewandelt.
Das Forschungsteam ist begeistert über die Einfachheit dieser Methode mit ihren verhältnismäßig geringen Anforderungen an wertvolle Proben und aufwändige Laborausstattung und erhofft sich ihre Verbreitung vom MPSD in Laboren weltweit.
Außer bei Proteinen und anderen Biomolekülen kann die serielle Elektronenbeugung auch für viele neuartige Funktionsmaterialien eingesetzt werden – wie zum Beispiel Perovskite und metallorganische Frameworks, die vielversprechende Kandidaten für zukünftige Anwendungen in Solarzellen und Wasserstoffspeichern darstellen.
Diese Newsmeldung wurde via Informationsdienst Wissenschaft erstellt.